近日,金萃媛博士联合广东省人民医院儿科杨敏团队在国际著名期刊《Advanced Science》(中科院一区TOP期刊,IF=14.3)合作发表了题为“Gut Dysbiosis Drives Inflammatory Bowel Disease Through the CCL4L2-VSIR Axis in Glycogen Storage Disease”的文章,这一突破性研究为糖原贮积病及其相关并发症的治疗提供了新的视角。
糖原贮积病(Glycogen storage disease, GSD)是一种罕见的遗传性代谢疾病,其主要原因是糖原在体内(主要是肝脏和/或肌肉)的不当储存,而编码葡萄糖-6-磷酸转移酶的基因(G6PT/SLC37A4)突变则会导致Ib型糖原贮积症(GSD-Ib)。GSD-Ib患者经常患有炎症性肠病(IBD),但其潜在的病因尚不明确。由于缺乏特异性的预警指标和精准有效的防治方案,临床管理极其艰难,GSD相关IBD不仅严重影响患儿的生命安全和生活质量,也给家庭和社会带来沉重的经济和医疗负担。
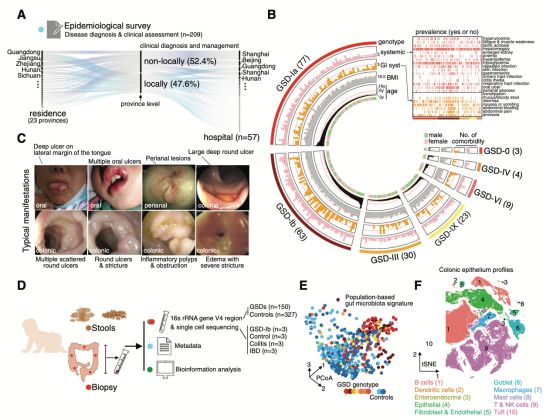
通过对150例GSD患儿、137例家庭对照和190例健康儿童进行研究,发现GSD-Ib患者常表现为单个或多发的深圆形溃疡、炎症假息肉、梗阻和狭窄,与典型的IBD显著不同。GSD患者的肠道微生态和结肠黏膜单细胞测序分析显示,GSD导致的口腔病源性潜在致病菌是肠道微生物群不成熟和结肠巨噬细胞积聚的主要诱因。特别是在肠道中,对病原菌的反应识别出一种高表达CCL4L2的独特巨噬细胞亚群。CCL4L2-VSIR轴的激活导致上皮细胞中AGR2和ZG16表达增加,介导了GSD-Ib中IBD的特异性进展。总的来说,该研究不仅证明了GSD相关IBD的微生物群驱动病理机制,还揭示了CCL4L2-VSIR轴在肠黏膜免疫调控及肠屏障功能中的关键作用。因此,针对肠道菌群失调及CCL4L2-VSIR轴或可成为治疗GSD相关IBD的一种潜在靶点,有望为这一罕见疾病的治疗带来突破性的进展。
论文链接:https://doi.org/10.1002/advs.202309471