人口老龄化加剧已成为全球的共性问题,预计到2030年全球60岁以上人口将至少达到21亿。由于年龄被认为是各种退行性疾病和慢性疾病的主要危险因素,因此在基于衰老机制研究基础上开发抗衰老疗法或预防措施迫在眉睫。近日,以我院自主培养的硕士研究生张海瑞为第一作者,在知名期刊Advanced Healthcare Materials(5年影响因子10.6)发表名为“Senolytic Therapy Enabled by Senescent Cell-Sensitive Biomimetic Melanin Nano-senolytics”的研究论文,报道了一种新的基于衰老细胞响应的“双锁和钥匙”可切换纳米前药,在治疗器官衰老和化疗引起的肿瘤衰老和进展中展现出令人兴奋的潜力。
细胞衰老被认为是机体衰老的主要标志,也是机体衰老的根本原因。细胞衰老是指一种细胞复制停滞,细胞周期相关抑制蛋白(如P53、P21和P16)高度表达,衰老相关β-半乳糖苷酶(SA-β-gal)水平升高的生理或病理状态,其特征性分泌大量促炎细胞因子、趋化因子和基质重塑酶,即衰老相关分泌表型(SASP),由此进一步引发无菌炎症、组织损伤、纤维化的发生和旁分泌导致的细胞衰老。衰老细胞(SnCs)的病理性积累会导致一系列与年龄相关的疾病,如癌症、肺纤维化、心血管疾病、神经退行性疾病和加剧的病毒感染。由此,开发可消除衰老细胞的衰老细胞清除剂(Senolytics)已成为预防、延缓或减轻衰老过程的一种切实可行的治疗策略。但是,传统衰老细胞清除剂(Senolytics)目前仍存在靶向性差、生物可容度低、清除效率不足等弱点。
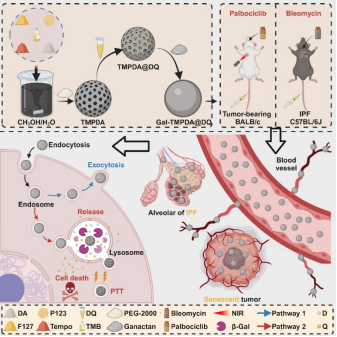
基于此,课题组开发了一种新型的清除衰老细胞的“Nano-Senolytics”药物,其特点是在经典衰老细胞清除药物(dasatinib+quercetin)基础上,构建了具有可调节通道的介孔框架和通过结合聚半乳糖衣和TMPDA的“双锁”智能表面修饰的纳米系统。研究证实,合成的Nano-Senolytic在消除SnCs方面显示了显著的特异性和有效性,在不影响正常组织的情况下逆转了小鼠的肺纤维化。结合光热效应,纳米粒子表现为高效去除化疗诱导的衰老肿瘤细胞,从而阻止了乳腺癌生长和转移。这一发现为衰老细胞的靶向治疗,以及延缓衰老或缓解年龄相关疾病的药物开发提供了一个新的、有应用潜力的技术体系。
该论文第一单位为浙江树人学院转化医学研究院,硕士研究生张海瑞和医学院徐晓玲副教授为论文共同第一作者,史丽云教授为通讯作者。论文得到国家自然科学基金资助。
原文链接:https://doi.org/10.1002/adhm.202401085