近日,史丽云教授团队在国际知名学术期刊Advanced Science(中科院一区,影响因子15.1)上在线发表题为“Defective Lamtor5 leads to autoimmunity by deregulating v-ATPase and lysosomal acidification”的文章,揭示了一条由Lamtor5介导的免疫调控新机制及其在自身免疫性疾病中的作用。
系统性红斑狼疮(SLE)是以免疫性炎症为突出表现的自身免疫性疾病,常累及多系统、多器官,其发病机制复杂,临床治疗面临巨大的挑战。巨噬细胞在SLE的发生、发展过程中发挥重要调控作用。巨噬细胞的溶酶体酸性或功能过强,会引发异常的抗原提呈过程,导致SLE发生;而巨噬细胞中溶酶体酸性或功能受损,则导致抗原/抗体复合物在体内的累积,亦可引发和加重SLE表型。因此,实现巨噬细胞中溶酶体酸性的精确调控在治疗自身免疫性疾病中的具有较强的潜力。课题组在自主构建Lamtor5髓系条件性敲除小鼠模型基础上,结合临床样本检测和转录组学、溶酶体功能分析、分子对接等多种技术手段,首次报道了一个新的参与SLE发生、发展的分子�——Lamtor5,阐明了其通过调节溶酶体质子泵v-ATPase参与免疫自稳的机制。
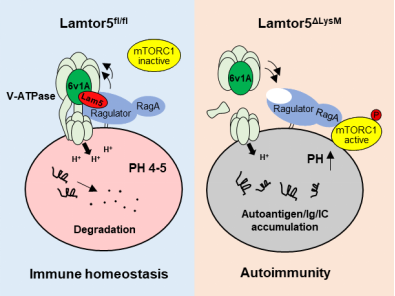
研究表明,巨噬细胞Lamtor5通过与v-ATPase的ATP6V1A亚基相互作用,稳定v-ATPase的组装和溶酶体的酸化,抑制异常活化的mTORC1信号通路,从而促进抗原/自身抗体复合物的清除,改善系统性红斑狼疮的症状。由此,髓系条件性敲除Lamtor5小鼠出现自发狼疮样表型和系统性炎症;临床上,SLE患者外周血单个核细胞(PBMCs)中Lamtor5的表达显著低于健康人,且与疾病进展密切相关。课题组据此开发了基于Lamtor5拯救和mTORC1通路阻断的技术方法,显著改善SLE小鼠症状的作用,从而为相关疾病的防治提供了一个有应用潜力的分子靶点和技术手段。
该研究获得国家自然科学基金项目(822770014, 81991523, 82371812, 82000014)、国家重点研发计划项目(2018YFC1705900)等项目资助。
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/advs.202400446